Theo GS Trương Việt Dũng, Chủ tịch Hội đồng Đạo đức, việc có cấp phép khẩn cấp cho vaccine Nano Covax hay không là quyết định của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, Hội đồng Đạo đức chỉ là bên đưa ra ý kiến tư vấn. Tuy nhiên việc vaccine Nano Covax được chấp thuận kết quả thử nghiệm lâm sàng giữa kỳ pha 3a là cơ sở quan trọng để vaccine được xem xét cấp phép khẩn cấp.
PGS-TS Lê Văn Truyền, Chủ tịch Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, Bộ Y tế cho biết, sau khi nhận được hồ sơ về kết quả thử nghiệm lâm sàng giữa kỳ pha 3a vaccine Nano Covax, theo kế hoạch vào ngày mai 29-8, Hội đồng sẽ họp xem xét đề nghị cấp phép khẩn cấp cho vaccine này. Đồng thời, Công ty Nanogen cũng cần hoàn thiện toàn bộ hồ sơ đăng ký lưu hành vaccine Nano Covax gửi Cục Quản lý Dược.
Theo quy định, trong thời hạn tối đa 20 ngày kể từ ngày nhận đủ hồ sơ đề nghị cấp giấy đăng ký lưu hành vaccine, Cục trưởng Cục Quản lý Dược sẽ cấp giấy đăng ký lưu hành vaccine. Việc cấp phép sẽ dựa trên quy định của Thông tư 11 về Hướng dẫn đăng ký lưu hành vaccine Covid-19 trong trường hợp cấp bách vừa được Bộ Y tế ban hành vào ngày 19-8.
Theo đó, vaccine đủ tiêu chuẩn cấp phép khẩn cấp có điều kiện khi đang thử nghiệm lâm sàng và đã có kết quả thử nghiệm giữa kỳ pha 3a về tính an toàn và hiệu quả bảo vệ của vaccine dựa trên dữ liệu về tính sinh miễn dịch của vaccine. Đồng thời, việc cấp phép sẽ dựa trên ý kiến tư vấn của Hội đồng Đạo đức trong nghiên cứu y sinh học cấp quốc gia và ý kiến tư vấn của Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc, có tham khảo hướng dẫn hoặc khuyến cáo của Tổ chức Y tế Thế giới.
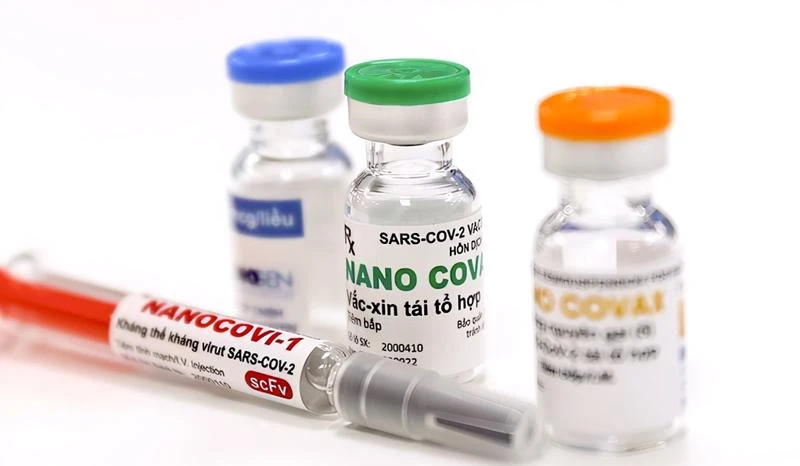
Kết quả đánh giá giữa kỳ giai đoạn 3a cho thấy, vaccine Nano Covax có tỉ lệ chuyển đổi huyết thanh lên tới 99,2% ở ngày thứ 42. Gộp chung giai đoạn 2 và 3a, nhóm nghiên cứu kết luận trung bình nhân nồng độ kháng thể tăng gấp 218,93 lần sau 42 ngày tiêm vaccine. Tỉ lệ chuyển đổi huyết thanh đạt 99,2%. Với kết quả này, vaccine Covid-19 Nano Covax đạt yêu cầu về tính sinh miễn dịch và tiếp tục thực hiện nghiên cứu giai đoạn 3b trên 12.000 tình nguyện viên.
Cùng với việc xem xét hồ sơ vaccine Nano Covax, trong ngày mai 29-8, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc sẽ xem xét hồ sơ xin cấp phép khẩn cấp của vaccine Hayat-Vax ngừa Covid-19 được sản xuất tại Các Tiểu vương quốc Ả Rập thống nhất (UAE). Đây là vaccine được hợp tác, chuyển giao công nghệ với Sinopharm của Trung Quốc.
Trước đó, Công ty CP Y dược phẩm Vimedimex đã đề nghị lên Thủ tướng Chính phủ xem xét, chấp thuận và chỉ đạo Bộ Y tế thẩm định nhanh hồ sơ đăng ký khẩn cấp vaccine Covid-19 Hayat-Vax cho nhu cầu phòng chống dịch bệnh.
| Đạt yêu cầu về tính an toàn và sinh miễn dịch Vaccine Nano Covax sử dụng công nghệ protein tái tổ hợp là vaccine đầu tiên của Việt Nam hiện đang thử nghiệm lâm sàng giai đoạn 3. Kể từ khi bắt đầu thử nghiệm lâm sàng (tháng 12-2020) đến nay đã tiêm cho khoảng 14.000 tình nguyện viên. Trong đó, giai đoạn 3a thử nghiệm trên 1.004 tình nguyện viên ở Hà Nội và Long An.
|
| Mới đây, Hãng Dược HLB của Hàn Quốc đã ký biên bản ghi nhớ (MOU) với Công ty Nanogen để mua quyền cung cấp vaccine Nano Covax trên toàn cầu (ngoại trừ tại Việt Nam và Ấn Độ). Hai bên dự định hoàn tất quá trình đàm phán sau khi các nhà khoa học đại diện của mỗi bên hoàn tất việc xem xét dữ liệu lâm sàng về vaccine Nano Covax trong 3 tháng tới. Trước đó, tại Đại sứ quán Việt Nam tại Ấn Độ đã diễn ra buổi ký kết hợp đồng bảo mật giữa Công ty Vekaria Healthcare LLP của Ấn Độ và Công ty Nanogen của Việt Nam nhằm phục vụ chuyển giao công nghệ, sản xuất và phân phối vaccine Nano Covax. |