Theo ông Phan Trọng Lân, Cục trưởng Cục Y tế dự phòng, với vaccine Pfizer, từ ngày 22-8 đã được Cơ quan Quản lý dược và thực phẩm Hoa Kỳ (FDA) và Cơ quan Quản lý dược châu Âu (EMA) thông qua hạn sử dụng từ 6 tháng lên 9 tháng. Có nghĩa 2 lô vaccine Pfizer 124001 và 123002 nhập về Việt Nam còn hạn sử dụng 3 tháng.
Ông Phan Trọng Lân khẳng định, việc tăng hạn sử dụng của vaccine được dựa trên kết quả nghiên cứu độ ổn định theo hướng dẫn đối với thuốc mới cũng như sản phẩm sinh học. Nghiên cứu được tiến hành trên các dải nhiệt độ bảo quản khác nhau, kết quả cho thấy vaccine đã có độ ổn định, đảm bảo chất lượng, hạn dùng đến 9 tháng kể từ ngày sản xuất. Hơn nữa, việc gia hạn sử dụng này được áp dụng chung trên toàn cầu và được sử dụng cho tất cả các đối tượng, bao gồm trẻ từ 12 tuổi trở lên. Việc gia hạn này cũng đã được kiểm định khắt khe và đảm bảo chất lượng an toàn, hiệu quả.
Cục trưởng Cục Y tế dự phòng cũng cho biết, các lô vaccine Pfizer có hạn sử dụng 6 tháng thì tự động tăng hạn dùng lên 9 tháng sau thời gian FDA và EMA phê duyệt kể trên. Trên cơ sở kết luận của FDA và EMA, ngày 30-9, Hội đồng tư vấn cấp số đăng ký lưu hành thuốc của Việt Nam đã chính thức thông qua việc kéo dài hạn sử dụng đối với vaccine của Pfizer từ 6 tháng lên 9 tháng.
Tiếp đó, ngày 22-10, Cục Quản lý dược, Bộ Y tế đã có văn bản đồng ý về việc tăng hạn dùng của vaccine Covid-19 Pfizer. Theo đó, các lô vaccine Pfizer được nhập về Việt Nam sau ngày 22-10 với hạn dùng 6 tháng in trên nhãn thì tự động tăng thêm 3 tháng. Như vậy, 2 lô vaccine 124001 và 123002 sẽ có hạn dùng đến ngày 28-2-2022.
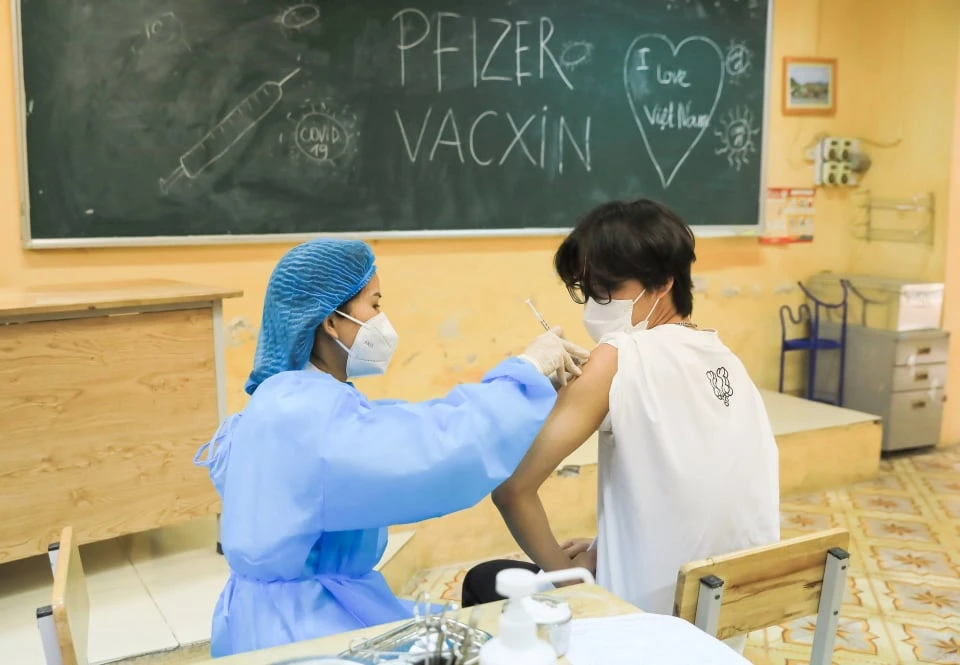 Tiêm vaccine Pfizer cho học sinh THPT tại Hà Nội. Ảnh: VIẾT CHUNG
Tiêm vaccine Pfizer cho học sinh THPT tại Hà Nội. Ảnh: VIẾT CHUNG Trước đó, ngày 20-9 và 6-10, Cục Quản lý dược nhận được các văn bản của Công ty TNHH Pfizer (Việt Nam) về việc đề nghị tăng hạn dùng của vaccine Pfizer từ 6 tháng lên 9 tháng ở điều kiện bảo quản -90°C đến -60°C.
Đến ngày 22-10, Cục Quản lý dược có văn bản gửi Công ty TNHH Pfizer đồng ý về việc này. Đồng thời, yêu cầu Công ty TNHH Pfizer (Việt Nam) phải chịu trách nhiệm về chất lượng đối với vaccine lưu hành trên thị trường và có trách nhiệm thông báo sự thay đổi này đến các đơn vị liên quan.
Cục Quản lý dược cũng nhấn mạnh việc tăng thời hạn sử dụng đối với vaccine Pfizer được dựa trên hướng dẫn của FDA và EMA.
Cũng liên quan vấn đề này, ngày 29-11, Công ty TNHH Pfizer (Việt Nam) có văn bản gửi Viện Kiểm định Quốc gia vaccine và sinh phẩm y tế xác nhận hạn dùng của 2 lô vaccine Pfizer số 124001 và 123002 sẽ có hạn dùng tăng 3 tháng so với hạn dùng in trên nhãn.
Về phía Viện Vệ sinh dịch tễ Trung ương đã chỉ đạo hệ thống tiêm chủng trên cả nước thông báo việc tăng hạn sử dụng 2 lô vaccine trên để tiêm cho trẻ 12-17 tuổi.